Содержание:
- 1 Причины дрожжевой инфекции
- 2 Симптомы хронической дрожжевой инфекции
- 3 Как вылечить хроническую дрожжевую инфекцию?
- 4 Содержание
- 5 Жизненный цикл [ править | править код ]
- 6 Научное значение [ править | править код ]
- 7 Использование в качестве пробиотика [ править | править код ]
- 8 Saccharomyces cerevisiae, как возбудитель болезней у людей [ править | править код ]
 Большинство взрослых женщин не понаслышке знакомо с дрожжевыми инфекциями и многие пытаются их победить годами. Чаще всего это вагинальные кандидозы, в просторечье именуемые молочницей, к которым почему-то относятся как-то поверхностно, даже легкомысленно. Хотя это отнюдь не весело, потому что даже самая безобидная вспышка активности дрожжевых грибков причиняет дискомфорт, да и лечится все это не так просто и быстро, как уверяет реклама препаратов от молочницы. А определить, а затем и вылечить хроническую дрожжевую инфекцию сложно вдвойне, потому что необходимо изменить образ жизни.
Большинство взрослых женщин не понаслышке знакомо с дрожжевыми инфекциями и многие пытаются их победить годами. Чаще всего это вагинальные кандидозы, в просторечье именуемые молочницей, к которым почему-то относятся как-то поверхностно, даже легкомысленно. Хотя это отнюдь не весело, потому что даже самая безобидная вспышка активности дрожжевых грибков причиняет дискомфорт, да и лечится все это не так просто и быстро, как уверяет реклама препаратов от молочницы. А определить, а затем и вылечить хроническую дрожжевую инфекцию сложно вдвойне, потому что необходимо изменить образ жизни.
Знать, чтобы победить: что такое дрожжевая инфекция?
Дрожжи, которые вы покупаете в магазине, чтобы испечь пирожки, и дрожжевая инфекция (молочница) – родственники. В обширной семье дрожжей – одноклеточных грибов — таких «родственников» почти 600 родов, но только один из них – Candida Albicans – виновен во всех мучениях, которые вам причиняет молочница.
Кстати, пищевые, то есть пекарские, дрожжи, которые являются источником витаминов группы В и аминокислот, это вид Saccharomyces CEREVISIAE и он никак не способствует развитию Candida. Мало того, многие натуропаты рекомендуют использовать в приготовлении пищи и для различных масок для лица и волос именно пекарские дрожжи.
Дрожжи в вашем теле
Практически каждый человеческий организм «сожительствует» с дрожжевыми грибками помимо сотен видов других микроорганизмов. Дрожжи находятся в полости рта, в пищеварительном тракте, на коже и слизистых (там же, кстати, в случае чего и появляются очаги кандидоза – стоматиты, молочница, кандидозы легких, кожи или кишечника). В здоровом организме такое «общежитие» находится в уверенном равновесии — симбиозе. Микроорганизмы живут, как соседи по многоэтажке – относительно мирно, но каждый занят своим делом и не залезает на территорию соседа. Однако вдруг это равновесие нарушится…

Если вы когда-нибудь принимали антибиотики, то, скорее всего, после курса лечения столкнулись с молочницей, и на собственном опыте знаете, насколько ценным может быть это хрупкое равновесие. Самое печальное то, что после вроде бы благополучно вылеченной молочницы рецидивы дрожжевой инфекции следуют один за другим – крайне редко удается избавиться от Candida Albicans в первого раза и навсегда, то есть загнать дрожжевой грибок в приличные рамки того самого равновесия.
Все это происходит потому, что антибиотики убивают не только болезнетворные бактерии (то есть борются с заболеванием, против которого их и прописал врач), антибиотики как напалмом проносятся по всем микроскопическим жителям вашего организма… Кроме грибов, которые антибиотики не любят, но не особенно боятся.
А что сделает большая цыганская семья, если вдруг все их соседи по дому внезапно пропадут, оставив квартиры нараспашку? Правильно, они рано или поздно заселятся в эти квартиры, и будут там плодиться и размножаться. Именно так и делают грибы вида Candida Albicans. И очень скоро их становится много, очень много. И если даже соседи по дому вдруг захотят вернуться, будет уже некуда.
- Лечение дрожжевой инфекции – комплексное и длительное, которое не терпит промашек и легкомысленного подхода. Но это понимают далеко не все и не всегда. По статистике, больше половины людей живут с хронической дрожжевой инфекцией, даже не подозревая, кто истинный виновник их плохого самочувствия и усталости.
Причины дрожжевой инфекции
Для того чтобы определить, что же стало причиной активизации дрожжевых грибков – то есть что вызвало молочницу, надо понять, что именно разрушило баланс. А его, к сожалению, разрушить куда проще, чем восстановить.

Причинами дрожжевых инфекций могут быть:
- Практически все активные лекарственные препараты: кроме антибиотиков, это стероиды, гормоны, противозачаточные таблетки и много других;
- Неправильное питание, слишком много сладкого и жирного;
- Ослабление иммунной системы;
- Аллергии;
- Токсины в еде, питье или окружении;
- Паразиты;
- Стресс;
- Хлор в водопроводной воде;
- Химическая чувствительность.
Если какая-то из причин постоянно воздействует на ваш организм, высок шанс развития хронической дрожжевой инфекции. Она будет протекать совсем не так, как острая – с зудом, творожистым белым налетом и гнилостным запахом, этих проявлений, скорее всего и не будет; все будет куда скромнее, незаметнее и … опаснее.
Симптомы хронической дрожжевой инфекции
Таким образом, если у вас нет активной дрожжевой инфекции, можете ли вы утверждать, что не страдаете от хронического кандидоза?

Люди с хроническими дрожжевыми инфекциями могут иметь один или несколько следующих симптомов:
- Усталость после еды;
- Проблемы с кишечником — запор, диарея, др.;
- Чувство гнева, депрессии, агрессии, тревоги после еды;
- Перепады настроения;
- «Туман» в мозгу, нежелание размышлять;
- Желание съесть что-то сладкое;
- Анальный зуд;
- Кожные инфекции;
- ПМС;
- Потеря памяти;
- Ночная потливость;
- Пищевые аллергии;
- Головокружения;
- Рецидивирующие грибковые инфекции, например, между пальцами ног или на стопах;
- Боль в суставах;
- Гиперчувствительность к экстремальным условиям – к жаре или холоду;
- Хронические боли;
- Изжога.
«Разрастание» Candida Albicans и перетекание острого кандидоза в хроническую дрожжевую инфекцию может провоцировать много тяжелых состояний, как то: синдром раздраженной толстой кишки, алкоголизм, тревожные расстройства, рассеянный склероз, астма и целый ряд других аутоиммунных заболеваний.
Тест на хроническую дрожжевую инфекцию в домашних условиях
Если у вас нет активной молочницы, то ходить к врачу бессмысленно – анализы, соскобы и мазки ничего не покажут. Но существует простой, доступный и в домашних условиях тест, который можно выполнить без участия медработников.
В народе его называют «тест по плевку»: возьмите стакан с водой комнатной температуры (вода должна быть чистой, без газа, не минеральной и не кипяченой) и… плюньте в воду. Это надо сделать утром, сразу после пробуждения, прежде чем вы положите что-либо в рот – и до чистки зубов, и до первого глотка воды, вообще до всего. Проверяйте стакан с водой каждые 15 минут.
Если у вас есть скрытая дрожжевая инфекция, вы увидите что-то из этого:
- Слюна растечется по всей поверхности воды до стенок стакана;
- Слюна распадется на капли, взвешенные в воде;
- Облачко слюны будет опускаться или опустится на дно стакана.
Если же слюна останется плавать на поверхности воды без каких-либо изменений на протяжении как минимум часа, то хронический кандидоз, скорее всего, не ваша проблема.
Как вылечить хроническую дрожжевую инфекцию?
Лечение и профилактика молочницы, по большому счету, состоит из двух этапов – вы убираете питательную среду и подселяете агрессивных соседей, которые будут держать ваших «цыган» в рамках приличия.
Этап №1: диета при лечении хронической дрожжевой инфекции
Главное в лечении хронической молочницы – разумное питание. Дрожжи чувствительны к продуктам, которые вы постоянно потребляете: например, хроническая дрожжевая инфекция процветает на сахаре, уксусе (кроме натурального яблочного уксуса), алкоголе и простых углеводах (это хлебобулочные изделия, сдоба, макароны).

Потребляйте больше сырых фруктов и овощей, ешьте больше зелени и орехов, цельнозерновых и растительных масел. Внимательно относитесь к выбору продуктов животного происхождения, интересуйтесь, откуда мясо, где выросла эта курица, и покупайте яйца домашних кур, которых живут на свободном выгуле.
Если вы откажетесь от некоторых продуктов, вы сможете легко контролировать Candida Albicans, а, значит, вылечить и хроническую молочницу.
Не стоит употреблять:
- Все виды сахара, включая мед и фруктозу;
- Обработанные продукты (снеки, фаст-фуд, газировка и т.п.);
- Кофеин;
- Пшеницу, рожь и ячмень;
- Простые углеводы — хлеб, белый рис, макароны, которые сразу же распадаются до простых сахаров в организме;
- Молочные продукты — они содержат простые сахара;
- Алкогольные напитки;
- Уксус;
- Продукты животного происхождения – есть риск, что при выращивании животных использовались антибиотики, особенно важно отказаться от бройлерной птицы и яиц;
- Сою и соевые продукты – они могут воздействовать на гормональный баланс и привести к усилению хронической дрожжевой инфекции;
- Вино и пиво.
Как быть с таблетками?
Важно свести к минимуму прием лекарств и пользоваться для купания и приготовления пищи не хлорированной водой. Даже противозачаточные таблетки могут провоцировать гормональный дисбаланс, который поддерживает молочницу. Попробуйте перейти на негормональные средства контрацепции.
Этап №2: полезные бактерии
Согласитесь, если соседи никуда не пропадут, цыгане вряд ли отважатся занимать их квартиры. Или если соседи вернутся с превосходящими силами, то захватчики их территории с извинениями ретируются.
- Поддерживайте здоровую микрофлору кишечника. При рациональном питании, на самом деле, это совсем не тяжело – растительная пища очистит кишечник, стабилизирует его работу.
- Отсутствие «мусорной» еды, содержащей гормоны, антибиотики, химические вещества разного уровня токсичности, оздоровит тело, но ему желательно дополнительно помогать – принимайте пробиотики. Эти добавки содержат живые организмы, которые приживаются в кишечнике, и поддерживают здоровье пищеварительной системы, контролируя разрастание дрожжей.
- Выбирайте те препараты, которые помимо непосредственно ПРОбиотических бактерий содержат ПРЕбиотические ингредиенты, которые помогают полезным бактериям расти.
В гастроэнтерологии, как и в других областях медицины, динамично развиваются методы диагностики и лечения грибковых инфекций на основе изучения физиологии, микробиологии, фармакологии, молекулярной патологии и медицинской генетики. Детально изучаются уже
В гастроэнтерологии, как и в других областях медицины, динамично развиваются методы диагностики и лечения грибковых инфекций на основе изучения физиологии, микробиологии, фармакологии, молекулярной патологии и медицинской генетики. Детально изучаются уже известные варианты болезни и описываются редкие и новые нозологические формы.
Грибы, являясь нормальными комменсалами желудочно-кишечного тракта (ЖКТ), становятся патогенными при определенных условиях. Это касается в основном дрожжеподобных грибов Candida spp., виды и даже штаммы которых различаются по факторам агрессии, способности к адгезии и инвазии [15].
Candida albicans — наиболее частый возбудитель кандидоза ЖКТ. Однако в последние годы большую роль играют Candida non-albicans (C. krusei, C. tropicalis, C. kefyr, C. glabrata, C. parapsilosis); у лиц с иммунодефицитом их пропорция составляет более 50%, при «относительно нормальном» иммунитете — 15%.
Грибы Candida (условно-патогенные микроорганизмы) заселяют ЖКТ — этот феномен называется колонизацией, — процесс протекает бессимптомно. Исследование взрослых здоровых добровольцев показало, что Candida albicans присутствует в орофарингеальной зоне у 20–30% из них, в тонком кишечнике — у 50–54%, в толстом кишечнике — у 55–70% и в фекалиях — у 65–70% [9, 13]. При исследовании состава микрофлоры полости рта у населения нескольких стран Европы обнаружено присутствие грибов у 10–25% людей, в кале — у 65–80% [11, 17]. Детально изучена колонизация зева грибами Candida у больных гемобластозами: она составила 33% [8]. В биоптатах гастродуоденальных язв в 17–30% случаев находят дрожжеподобные грибы [12]. У 50% жителей Германии в микробиоте кишечника присутствуют грибы, а у онкогематологических больных колонизация кишечника составляет 63–65% [10, 11]. Нельзя забывать, что у 0,8–4% пациентов грибы случайно обнаруживаются в пузырной и протоковой желчи, а при желчнокаменной болезни — у 15–20%.
Бессимптомное пребывание грибов в ЖКТ может прекратиться, когда они приобретают патогенные свойства. Так, у больных с нейтропенией грибы из кишечника могут диссеминировать в печень, селезенку и легкие, а в катетер-ассоциированной ситуации грибы попадают непосредственно в ток крови, достигают сердца и почек.
Дрожжеподобный гриб Cryptococcus neoformans в патологии ЖКТ как этиологический фактор играет незначительную роль. Он чаще поражает нервную систему и, диссеминируя из первичного очага, вовлекает гастроинтестинальный тракт. Описаны единичные случаи (чаще посмертно) криптококкового эзофагита, стоматита, терминального илеита, колита, холецистита, панкреатита. Как правило, они относились к ВИЧ-серопозитивным больным, а также к пациентам, страдающим гипергаммаглобулинемией Е с рецидивирующими абсцессами печени и перианальной зоны.
Болезни ЖКТ, вызванные диморфными патогенными грибами (II группы патогенности), зарегистрированы в Южной Америке, но время от времени встречаются как спорадические случаи по всему миру. Большинство диморфных грибов в природе существуют в мицелиальной форме, попав в организм они трансформируются в дрожжеподобные и приобретают патогенные свойства. Пероральный путь проникновения не характерен, в ЖКТ эти грибы попадают при диссеминации из других органов. Blastomyces dermatitidis продуцирует гранулематозное повреждение в желудке и тонком кишечнике. Coccidioides immitis, Histoplasma capsulatum, Paracoccidioides brasiliensis и Sporothrix schenckii поражают кишечник только при диссеминации из кожных очагов и респираторного тракта [6, 15].
Грибы Aspergillus spp. редко вызывают болезнь ЖКТ, только в случаях стойкой нейтропении, кахексии и при других отягощающих состояниях.
Грибы класса Zygomycetes могут привести к развитию интестинального зигомикоза, который, как правило, ассоциирован с амебиазом, голоданием, диабетическим кетоацидозом, почечным гемодиализом. Penicillium spp. и Geotrichum поражают ЖКТ также редко.
Дрожжеподобные, плесневые и некоторые диморфные грибы — это условно-патогенные, оппортунистические микроорганизмы, которые широко распространены в окружающей среде и легко могут попадать на кожу, слизистые оболочки полости рта, гениталий и в дыхательные пути. Кроме того, для грибов характерен эндогенный способ существования (миконосительство).
ЖКТ покрыт слизистой оболочкой, состоящей из двух компонентов — поверхностного скользкого, слизистого слоя, по которому микроорганизмы легко продвигаются вдоль всего ЖКТ, и более глубокого плотного гликопротеинового слоя с остатками сиаловой кислоты, который формирует физиологический барьер. Адгезия и последующая инвазия грибов через этот плотный слой возможны только благодаря продукции грибами протеолитических «ферментов инвазии»: коагулазы, каталазы, козеиназы, фосфолипазы, а также фибриллярных протеиновых комплексов и эндотоксинов [15].
При физиологическом благополучии между макро- и микроорганизмами существует определенное равновесие, в котором играют роль, с одной стороны, факторы устойчивости организма к микроскопическим грибам, а с другой — факторы патогенности грибов.
Устойчивость организма зависит от принадлежности к группам риска и состояния иммунной системы.
Перечислим факторы риска развития грибковых инфекций ЖКТ.
- Поражение слизистых оболочек полости рта (красный плоский лишай, зубные протезы, травмы, ксеростомия, использование гормональных ингаляторов).
- Хронические заболевания ЖКТ (атрофический гастрит, гипоацидность желудка, ахалазия, бульбит, эрозивно-язвенные заболевания пищевода и кишечника, дивертикулез, полипоз, гастроэзофагальная рефлюксная болезнь, энтероколит, болезнь Крона, синдром раздраженной кишки, обсемененность желудка Helicobacter pylori, дисбиоз, микст-инфекция кишки).
- Травмирование слизистой оболочки (ожоги, пищеводно-желудочный зонд, эндотрахеальная интубация).
- Беременность.
- Период новорожденности (недоношенность, массивность инфекции при прохождении через родовые пути, естественное несовершенство иммунной системы).
- Пожилой возраст (старение иммунной системы, сопутствующие заболевания, уменьшение амплитуды продольных сокращений пищевода, силы сокращений сфинктеров, нарушение процессов всасывания и т. д.).
- Онкологические и гематологические заболевания (нейтропения).
- Эндокринопатии (особенно сахарный диабет).
- СПИД, ВИЧ-инфицированность.
- Трансплантационные операции.
- Состояния, требующие пребывания в отделениях интенсивной терапии.
- Тяжелые аллергические заболевания.
- Прием антибиотиков, цитостатиков, гормонов и других химиопрепаратов в неадекватных дозах.
- Нарушения питания, в том числе голодание с целью снижения веса.
- Алкоголизм, курение, наркомания.
Важным компонентом защиты от инвазии ЖКТ является иммунная система, ассоциированная с кишечником. Клеточная часть этой системы включает в себя интраэпителиальные лимфоциты, которые препятствуют дисперсии возбудителя через lamina propria и агрегации в пейеровых бляшках. В-лимфоциты кишечника участвуют в продукции секреторных IgA и IgM, которые уменьшают способность грибов к адгезии.
Т-клетки здорового организма продуцируют защитный интерферон, усиливают фагоцитоз, активируют Т-цитотоксические лимфоциты. СД4 и СД8 укрепляют местный иммунитет в ЖКТ. Причем оказалось, что цитотоксичность СД8 играет более существенную роль в предотвращении заболевания, чем предполагали раньше.
В защите важны также макрофагальный и нейтрофильный фагоцитоз, препятствующие диссеминации грибковой, особенно кандидозной инфекции.
У ВИЧ-пациентов и больных с нейтропенией, у которых фагоцитоз резко подавлен, местная инвазия и диссеминация инфекции наступают очень быстро. Известно, что нейтрофилы хотя и не могут полностью защитить слизистую оболочку ЖКТ от «атаки» грибов, но благодаря собственной «киллерной» субстанции через специфический механизм запускают активацию комплемента, который усиливает фагоцитоз. Следует отметить, что фагоцитоз особенно важен при кандидозной инфекции, но «не работает» в тканях против капсулированных криптококков и большинства мицелиальных грибов.
Нормальные биохимические, гистохимические и физиологические процессы в ЖКТ, своевременная регенерация эпителиоцитов, кислотно-ферментативный барьер, полноценная перистальтическая активность также являются защитными факторами, которые препятствуют проникновению грибковой и бактериальной флоры [4]. Роль желудочной кислоты в предотвращении внедрения грибов в слизистую неоспорима. В среде с пониженной кислотностью грибы Candida приобретают патогенные свойства, появляются вегетирующие формы, образуется псевдомицелий или мицелий, повреждающий слизистую оболочку. У ВИЧ-инфицированных лиц, для которых характерна ахлоргидрия, попадающие с пищей грибы Candida могут вызывать кандидоз желудка, в то время как у людей с нормальным иммунитетом эта локализация встречается редко. Роль кислотности желудочного сока в развитии бактериальной и грибковой инфекции кишечника не подтверждена.
Облигатные микроорганизмы желудка и кишечника (аэробные лактобациллы, анаэробные бифидум-бактерии, нормальная кишечная палочка и др.) также играют защитную роль. Применение антибиотиков убивает, наряду с патогенными, и эти «полезные» бактерии, открывая на слизистой оболочке рецепторы адгезии для грибов [2].
Нельзя не упомянуть также о Helicobacter pylori, который довольно часто обитает в желудке, вызывает гастрит, язвенную болезнь, а иногда оказывает канцерогенное воздействие. В свою очередь, лечение хеликобактериоза антибиотиками приводит к активации грибов Candida и кандидозу желудка [1]. Ассоциации грибов с Helicobacter pylori и другими бактериями в ЖКТ встречаются нередко, что требует продуманного адекватного подхода к тактике лечения.
В желудке могут также присутствовать Saccharomyces cerevisiae и некоторые виды Candida, способные сбраживать и ферментировать до винного спирта сахара, попадающие с пищей в желудок. Этот феномен называется синдромом «пивоваренного завода» [14].
Вирулентность грибов, патогенные факторы, как и полисахариды (маннаны), плазмокоагулаза, эндотоксины, липиды, глюкоконъюгаты, влияют на развитие заболевания. Даже от внутривидовых способностей грибов зависит, разовьются ли в каждом конкретном случае кандиданосительство или болезнь [13]. Например, серотип В Candida albicans считается более вирулентным и наиболее распространенным возбудителем орофарингеального кандидоза у ВИЧ-инфицированных больных, также он поражает генитоуринарную систему и нередко выделяется из зева у гомосексуалистов.
Микроскопически факторы агрессии грибов Candida проявляются формированием ростковых трубок, псевдогифов и истинного мицелия — за счет них грибы могут врастать в стенку фагоцитов. Однако дрожжи, которые не способны продуцировать мицелий, такие, как Candida glabrata, Cryptococcus neoformans, также могут вызывать заболевания ЖКТ.
Диагностика
Тщательное изучение анамнеза, выявление факторов риска, хронических заболеваний ЖКТ, патогномоничных клинических симптомов играют большую роль в своевременности установления диагноза.
В последние годы за счет эндоскопических технологий расширились возможности диагностики грибкового эзофагита и гастрита. При эзофагогастродуоденоскопии обращают внимание на гиперемию и изъязвления слизистой, наличие белых налетов и «пленок», сужение просвета пищевода, скопление слизи. Во время этой процедуры в обязательном порядке следует брать материал для микробиологического исследования, так как не всегда этиология этих проявлений грибковая. Причем информативность исследования налетов выше, чем биоптатов (95% по сравнению с 39%).
Особенно перспективны видеоинформационные эндоскопические исследования с цифровой регистрацией и анализом изображения. Четкое разграничение неизмененных и патологических тканей, анализ гистохимических процессов в слизистой оболочке пищеварительного тракта возможны с помощью эндоскопической спектроскопии и флюоресцентной эндоскопии. Видео- и колоноскопия, хромоэндоскопия на фоне «лекарственного» сна по технологии «Диантек» имеют высокое качество исследования, безболезненность манипуляций и отсутствие стресса и страха у пациентов.
Следует, однако, подчеркнуть, что инвазивные манипуляции при воспаленной слизистой ЖКТ небезопасны, могут способствовать грибковой и бактериальной диссеминации, а иногда приводят к травме и перфорации стенки пищевода или желудка. Эндоскопическая ультрасонография с допплеровским картированием, контрастным усилением тканевых и сосудистых структур перспективна, она позволяет детально дифференцировать все слои стенки пищеварительного тракта. Неинвазивные методы — виртуальная эндоскопия, позволяющая получить трехмерное изображение, магнитно-резонансное исследование — имеют большое будущее [3].
Изучение гастродуоденальной моторики с помощью сцинтиграфии и электрогастрографии также важно для диагностики и назначения дополнительных лекарственных средств, так как нарушение двигательной функции желудка, «застой» в ЖКТ создают условия для размножения грибов и бактерий. Колоноскопия дает возможность оценить состояние слизистой кишечника, наличие белого налета, язвенных дефектов и т. д. В перспективе в гастроэнтерологии будут внедряться методы, в основе которых лежат новые научно-практические исследования: иммуноферментный анализ фекальных антигенов, ПЦР и даже генетическое тестирование [3].
Еще одним достаточно информативным методом в гастроэнтерологии является рентгенография пищевода, желудка и кишечника. Она дает возможность выявить дефекты наполнения (депо бария), изъязвления, деформацию, конвергенцию складок, изменения контуров и глубины перистальтики, сужение или расширение пищеводной трубки. С помощью рентгенографии желудка можно оценить его моторику, своевременность эвакуации пищевого комка, что важно для понимания патогенеза заболевания.
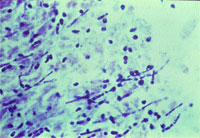 |
| Рисунок 1. Кандидозный эзофагит. Почкующиеся клетки и псевдогифы грибов Candida albicans на эзофагеальной язве |
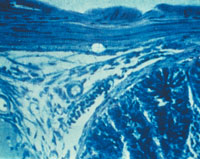 |
| Рисунок 2. Кандидозный энтерит. Утолщенные ворсинки и дефект слизистой тонкой кишки; псевдогифы грибов Candida |
Лабораторное подтверждение грибкового заболевания ЖКТ возможно при микроскопировании и/или культуральном исследовании смывов со слизистых оболочек полости рта и пищевода, содержимого желудка и кишечника, патологических «пленок», налетов и др. Количественная оценка грибов в биосубстратах должна проводиться в сопоставлении с клинической симптоматикой, с учетом наличия фоновых заболеваний, микст-инфекции и т. д. Например, обнаружение на слизистых единичных колоний Candida не является основанием для постановки диагноза «кандидоз» у иммунокомпетентных пациентов.
В кале диагностическую значимость приобретает количество колоний (более 10 5 –10 6 ). По-другому, с более низким диагностическим порогом, интерпретируются результаты посевов у иммуносупрессированных лиц, при нейтропении у больных СПИДом и в отделениях интенсивной терапии. Следует также обращать внимание на способность грибов к вегетации и образованию мицелия, так как это является одним из лабораторных признаков, подтверждающих диагноз кандидоза.
Гистологическое (окраска по Гомори–Гроккоту, ШИК-реакция) и цитологическое (окраска по Романовскому–Гимзе) исследования биоптатов позволяют обнаружить тканевые формы грибов. Многими авторами эти методы рассматриваются как наиболее достоверные. Кроме того, мицелий и псевдомицелий в тканях служат подтверждением наличия инвазивной формы грибковой инфекции ЖКТ (рис. 1, 2).
Кандидоз
Это наиболее распространенная грибковая оппортунистическая висцеральная патология. Агрессивные свойства грибов Candidа проявляются в их способности через стадию адгезии и инвазии поражать слизистые оболочки любых органов, в том числе и ЖКТ. Причем «атаке» подвергается чаще всего многослойный плоский эпителий полости рта и пищевода, реже — однослойный цилиндрический эпителий кишечника. Поэтому, как правило, в верхних отделах ЖКТ происходит инвазия грибов Candidа, а в отделах, расположенных ниже желудка, — колонизация. В то же время в кишечнике даже на стадии адгезии могут наблюдаться клинические симптомы — проявления неинвазивного кандидоза [10].
Язвенные дефекты пищевода, желудка и кишечника поддерживают грибковую колонизацию вплоть до инвазии. Желудочно-кишечный кандидоз нередко приводит к кандидемии.
Классификация кандидоза
I. Орофарингеальный кандидоз.
- Кандидоз полости рта у новорожденных.
- Псевдомембранозный кандидоз.
- Атрофический кандидоз полости рта (чаще у пожилых).
- Эритематозный кандидоз (новая форма).
- Срединный ромбовидный глоссит.
- Лейкоплакия, ассоциированная с кандидозом.
- Ангулярный кандидозный хейлит.
- Кандидозный гингивит (изолированно встречается редко).
II. Кандидозный эзофагит.
III. Кандидоз желудка.
- Эрозивно-фибринозный гастрит (диффузный).
- Вторичный кандидоз на фоне язвенной болезни.
- IV. Кандидоз кишечника.
- Псевдомембранозный.
- Коллагеновый.
- Лимфоцитарный.
V. Кандидозный проктосигмоидит.
VI. Перианальный кандидоз.
VII. Секреторная диарея, ассоциированная с кандидозом.
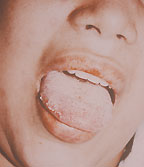 |
| Рисунок 3. Кандидозный глоссит. Типичные белые налеты и эрозии на воспаленной инфильтрированной слизистой |
Среди всех локализаций кандидоза пищеварительного тракта орофарингеальная занимает 1-е место (рис. 3).
О кандидозе полости рта упоминал еще Гиппократ, а впервые описал его хирург Лангенберк в 1839 г.
Кандидозный стоматит у новорожденных — распространенное заболевание. В первые дни после рождения слизистые ребенка устойчивы к грибам.
В дальнейшем недостаточная секреция IgA и постепенное снижение антимикробного иммунитета, переданного от матери, приводят к высокой заболеваемости. Патогномоничный синдром — белые творожистые налеты на слизистой полости рта, так называемая «молочница» [16].
Кандидоз ассоциирован также с ношением протезов. При этом развивается атрофический кандидоз, огромное количество грибов скапливается в щечных складках на фоне красного точечного воспаления слизистой; инвазия, как правило, отсутствует.
Кандидозный эзофагит в стационарах общего профиля встречается у 1,3–2,8% больных, в отделениях трансплантации — до 4%, при диссеминированном карциноматозе — от 2,8 до 6,7%. Это заболевание протекает часто без субъективных жалоб и выявляется случайно при «сплошных» исследованиях населения в 1–7% случаев [5, 17]. Иногда больные отмечают боль и дискомфорт при прохождении твердой и жидкой пищи, дисфагию, гиперсаливацию. По глубине поражения эндоскопически выделяют четыре типа — от легкого отека, гиперемии, единичных белых налетов
С. А. Бурова, доктор медицинских наук, профессор
Национальная академия микологии, ГКБ № 81, Москва
| Saccharomyces cerevisiae | |
|---|---|
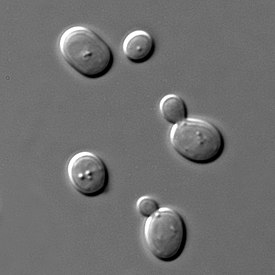 S. cerevisiae под микроскопом |
|
| Научная классификация | |
| Домен: | Эукариоты |
| Царство: | Грибы |
| Подцарство : | Высшие грибы |
| Отдел: | Аскомицеты |
| Подотдел : | Saccharomycotina O.E.Erikss. & Winka, 1997 |
| Класс: | Сахаромицеты ( Saccharomycetes G.Winter, 1880 ) |
| Порядок: | Сахаромицетовые |
| Семейство: | Сахаромицетовые |
| Вид: | Saccharomyces cerevisiae |
Saccharomyces cerevisiae Meyen ex E.C.Hansen 1883
Пекарские дрожжи [1] :96,102 (лат. Saccharomyces cerevisiae ) — вид одноклеточных микроскопических (5—10 мкм в диаметре) грибков (дрожжей) из класса сахаромицетов, широко используемый в производстве алкогольной и хлебопекарной продукции, а также в научных исследованиях. В 1996 году пекарские дрожжи стали первыми эукариотами, чей геном был полностью секвенирован [2] .
Содержание
Жизненный цикл [ править | править код ]
Клетки Saccharomyces cerevisiae размножаются вегетативным образом при помощи почкования. Сначала появляется вырост на материнской клетке, затем происходит митотическое деление ядра, образование клеточной стенки и отделение клеток друг от друга. На материнской клетке остается шрам от почкования, что позволяет определить её возраст. Обычно материнская клетка может образовывать 20—30 почек.
Клетки дрожжей могут пребывать в одном из двух стабильных состояниях (фазах): гаплоидном (сфероиды) и диплоидном (эллипсоиды), которые считаются различными поколениями. В течение каждой фазы пекарские дрожжи размножаются вегетативно почкованием. По продолжительности у пекарских дрожжей преобладает диплоидная фаза. Она переходит в гаплоидную фазу путём образования гаплоидных аскоспор в результате мейоза. Гаплоидная фаза переходит в диплоидную путём слияния образовавшихся из аскоспор гаплоидных клеток [1] :96-97 .
Для выращивания оптимальными условиями является раствор дрожжевого экстракта с температурой 30 °C, содержащий пептон и глюкозу.
Научное значение [ править | править код ]
Saccharomyces cerevisiae — один из наиболее изученных модельных организмов, на примере которого происходит исследование клеток эукариотов, они легко выращиваются и имеют низкую патогенность для человеческого организма. По сравнению с кишечной палочкой (Escherichia coli), клетка дрожжей содержит в несколько раз больше ДНК и имеет более сложную организацию, чем бактерии. Клетки сохраняют жизнеспособность даже с множественными генетическими маркерами в своем генотипе, что существенно с точки зрения генной инженерии [3] .
Использование в качестве пробиотика [ править | править код ]
Дрожжи Saccharomyces cerevisae используются в медицине и животноводстве в качестве пробиотика. В частности, в медицине нашёл применение штамм Saccharomyces cerevisae var. boulardii.
Ряд клинических исследований показал возможную пользу S. cerevisae var. boulardii для предотвращения или лечения некоторых кишечных заболеваний [4] . Имеются доказательства умеренного качества в пользу эффективности данного пробиотика для снижения риска диареи при лечении антибиотиками (как у детей, так и у взрослых) [5] [4] [6] , а также для снижения риска возникновения побочных эффектов при эрадикации Helicobacter pylori [7] [4] [6] . Кроме того, имеются некоторые данные в пользу эффективности S. cerevisae var. boulardii для предотвращения (но не лечения) «диареи путешественников» [4] [6] , а также в качестве вспомогательного средства при лечении острой диареи у взрослых и детей и хронической диареи у детей [4] .
Saccharomyces cerevisae var. boulardii считается безопасным в качестве лекарственного средства [6] . В ходе клинических испытаний этот пробиотик хорошо переносился пациентами, и частота нежелательных эффектов была сходной с их частотой в контрольных группах [5] . В ходе клинических испытаний не было зафиксировано ни одного случая фунгемии, вызванной этим микроорганизмом [6] .
В то же время в клинической практике отмечаются случаи фунгемии, вызванной Saccharomyces Cerevisiae и, в частности,Saccharomyces Cerevisiae var. boulardii [6] [4] . Группу риска составляют больные с иммунодефицитом, а также больные с центральным венозным катетером. Некоторые специалисты полагают, что S. Cerevisiae var. boulardii не следует использовать для лечения таких лиц [6] , тогда как другие считают, что необходимо только соблюдать должную осторожность [4] .
Saccharomyces cerevisiae, как возбудитель болезней у людей [ править | править код ]
Saccharomyces cerevisiae является оппортунистическим патогеном сравнительно низкой вирулентности [8] . Несмотря на широкое применение этого микроорганизма как в промышленности, так и в домашних условиях, случаи вызванных им инфекций встречаются нечасто [9] . Дрожжи данного вида встречаются на коже, на слизистых ротовой полости, глотки, желудочно-кишечного тракта и влагалища здоровых людей [10] . В частности, одна обзорная публикация, обобщившая данные ряда исследований, указывает на наличие S. cerevisiae в 6 % образцов, взятых из кишечника здоровых людей [11] . Некоторые специалисты считают S. Cerevisiae частью здоровой микрофлоры желудочно-кишечного тракта, дыхательных путей и влагалища человека [12] . Другие предполагают, что дрожжи этого вида, обнаруживаемые в организме человека, имеют внешнее происхождение (поступают с пищей) и могут задерживаться лишь в течение некоторого времени [13] [11] . Так, эксперименты показывают, что при намеренном приёме дрожжей данного вида здоровыми добровольцами, они исчезают из кишечника в течение пяти дней после прекращения приёма [11] [9] .
При определённых условиях, например, при снижении иммунитета, Saccharomyces cerevisiae может вызвать у человека инфекционное заболевание. В частности, данный грибок иногда вызывает у женщин вагинит. По данным ряда исследований доля вагинитов, вызванных S. cerevisiae, может составлять 0,45-1,06 % от всех случаев вагинита, вызванного дрожжевыми грибками. В некоторых случаях женщины, страдающие вагинитом, вызванным S. cerevisiae, находились в интимных отношениях с мужчинами, работающими в пекарнях или пиццериях, и было установлено совпадение штаммов S. cerevisiae из образцов из влагалища этих женщин, со штаммами, используемыми их интимными партнёрами в работе, причём образцы тех же штаммов были обнаружены и на руках мужчин. [8] В то же время отмечалось отсутствие в научной литературе (по состоянию на 1999 год) сообщений о подобном заболевании у женщин, которые сами работали в пекарнях [8] . Отдельные случаи вагинита, вызванного S. cerevisiae, связывались медиками с использованием дрожжей для домашней выпечки [8] . Также известны случаи инфекций ротовой полости и глотки, вызванных S. cerevisiae [8] .
Инвазивные и системные инфекции [ править | править код ]
В редких случаях Saccharomyces сerevisiae вызывает инвазивные инфекции (то есть заражает магистральный кровоток или другие жидкие среды организма, которые в норме должны быть стерильны, или внутренние органы, например, лёгкие, печень, селезёнку). Такая инфекция может стать системной, то есть затронуть несколько органов. Инвазивные микозы, вызванные Saccharomyces сerevisiae, — весьма опасны — смертность составляет более 30 % даже при проведении лечения. [8] [13]
По сравнению с инвазивными инфекциями, вызванными Cand >[8] [14] , даже у пациентов, ослабленных раковыми заболеваниями [14] . Так S. сerevisiae вызывает от 1 % до 3,6 % госпитальных фунгемий [13] .
Воротами инвазивной инфекции, вызванной Saccharomyces cerevisiae, могут стать: транслокация со слизистой (например, ротовой полости или кишечника) или загрязнённый венозный/артериальный катетер [12] . Предрасполагающими факторами для таких инвазивных инфекций являются: наличие венозного/артериального катетера, приём антибиотиков и иммунодефицит [13] , который может быть вызван, в частности, СПИДом, лейкемией или некоторыми медицинскими вмешательствами (например, трансплантацией костного мозга) [8] .
40 % инвазивных микозов, вызванных Saccharomyces cerevisiae, приходятся на штамм S. cerevisiae boulardii, используемый в качестве пробиотика [13] . Многие из этих случаев связаны непосредственно с намеренным медицинским употреблением S. cerevisiae boulardii, в других случаях имеет место госпитальная инфекция, связанная с занесением патогена в венозный/артериальный катетер через руки медицинского персонала либо, возможно, из воздуха, куда сухие дрожжи попадают при вскрытии пакетика с S. cerevisiae boulardii (когда медработник вскрывает пакетик, чтобы дать лекарство одному из пациентов, находящихся в палате) [15] [13] . По сравнению с другими штаммами S. cerevisiae штамм S. cerevisiae var. boulardii чаще вызывает инвазивные инфекции у людей, не страдающих иммунодефицитом [13] , хотя подобные осложнения являются очень редкими в практике терапевтического применения данного пробиотика [15] .
Известен случай, когда грибок Saccharomyces cerevisiae был обнаружен в одиночном лёгочном узле, хирургически удалённом из лёгкого человека, профессиональная деятельность которого была связана с регулярным пребыванием в различных пекарнях. Предполагается, что источником инфекции в данном случае стало вдыхание порошка сухих дрожжей. [16] [13] [10]
Сравнительная вирулентность различных штаммов [ править | править код ]
Вирулентность различных штаммов Saccharomyces cerevisiae — различна. Большинство штаммов, встречающихся в естественной среде, неспособны к росту при температурах выше 35 °C, характерных для тела человека и других млекопитающих. Вирулентные штаммы, однако, способны к росту при температурах выше 37 °C и часто до 39 °C, иногда даже до 42 °C. [10] Способностью к росту при температурах выше 37 °C обладают и некоторые штаммы, используемые в промышленности [8] . Согласно требованиям Европейского агентства по безопасности продуктов питания, штаммы Saccharomyces cerevisiae, способные к росту при температуре более 37 °C для того, чтобы получить презумпцию безопасности, должны не иметь резистентности к противогрибковым лекарственным препаратам [17] .
Способность к росту при сравнительно высоких температурах — не единственный фактор, влияющий на вирулентность штамма [10] .
Признаками вирулентности штамма Saccharomyces cerevisiae часто считают:
- способность выделять определённые энзимы, такие как протеиназа[8] и фосфолипаза[10] ;
- склонность к инвазивному росту (то есть к внедрению внутрь питательной среды) [10] ;
- способность к адгезии к клеткам млекопитающих [10] ;
- резистентность к воздействию перекиси водорода (перекись водорода выделяется макрофагами и играет роль в их воздействии на чужеродные микроорганизмы) [10] ;
- вообще резистентность к воздействиям со стороны иммунной системы человека или способность к воздействию на саму иммунную систему[10] .
Некоторые исследователи также считают признаком вирулентности способность к формированию псевдогиф [8] [10] , хотя другие полагают, что эта способность в одинаковой мере характерна как для вирулентных, так и невирулентных штаммов [10] .